METABOLISMO
A) Introduzione e generalità glicolisi
B) I Coenzimi
B) I Coenzimi
A)Introduzione: l'energia nelle cellule
La cellula, per soddisfare il proprio fabbisogno energetico, utilizza l'ossidazione del glucosio, una reazione fortemente esoergonica.
Questo carboidrato, in presenza di ossigeno, viene ossidato a CO2, mentre gli elettroni e gli ioni idrogeno che se ne ricavano, vengono utilizzati per la sintesi dell'ATP. L'elemento accettore finale di elettroni, cioè quello che si riduce, è l'ossigeno.
In sintesi:C6H12O6 + 6CO2 → 6CO2 + 6H2O + 2870 kjoule/mol
La cellula, per soddisfare il proprio fabbisogno energetico, utilizza l'ossidazione del glucosio, una reazione fortemente esoergonica.
Questo carboidrato, in presenza di ossigeno, viene ossidato a CO2, mentre gli elettroni e gli ioni idrogeno che se ne ricavano, vengono utilizzati per la sintesi dell'ATP. L'elemento accettore finale di elettroni, cioè quello che si riduce, è l'ossigeno.
In sintesi:C6H12O6 + 6CO2 → 6CO2 + 6H2O + 2870 kjoule/mol
Gicolisi e Respirazione cellulare
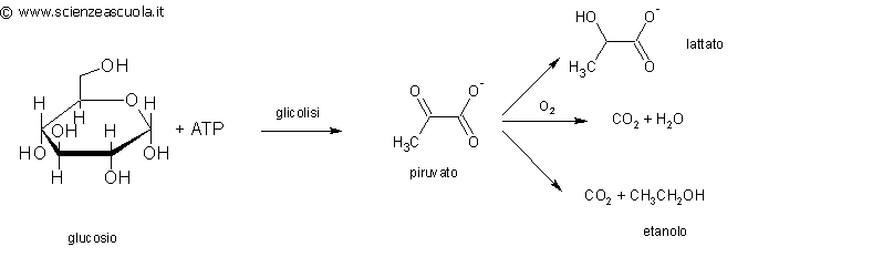
Questa reazione viene svolta dalla cellula in stadi diversi, in modo tale che l'energia venga liberata un po' alla volta, con grande efficienza. Infatti, il rendimento, che si calcola dal rapporto tra energia ottenuta ed energia totale, è circa 0,4, cioé il 40%.L 'ossidazione del glucosio si attua in due fasi:
- la glicolisi (nel citosol)
- la respirazione cellulare (nei mitocondri), che si divide a sua volta in ciclo di Krebs (anche noto come ciclo degli acidi tricarbossilici) e trasporto finale degli elettroni.
Entrano in gioco delle molecole trasportatrici di elettroni, i coenzimi:NAD+ (nicotinammide adenina dinucleotide ossidato) che, accettando un protone più due elettroni, si riduce a NADH(nicotinammide adenina dinucleotide ridotto);FAD (flavin adenina dinucleotide ossidato) che, accettando due protoni più due elettroni (in pratica due atomi di idrogeno), si riduce a FADH2 (flavin adenina dinucleotide ridotto).Nello stadio finale della respirazione, NADH e FADH2 cedono i loro elettroni alla catena di trasporto.
Questi ultimi vengono fatti scendere a livelli energetici via via più bassi, fino alla fase finale, dove si combinano con l'O2 e gli H+ per dare H2O.Questa serie di reazioni ha, come scopo ultimo, la sintesi di ATP da ADP e Pi (fosfato inorganico).Le reazioni della respirazione cellulare avvengono in presenza di ossigeno (aerobiosi) e producono 38 molecole di ATP.In assenza di ossigeno (anaerobiosi) avviene la fermentazione, che produce solo 2 molecole di ATP per ogni molecola di glucosio.
La glicolisi nel dettaglio
Glicolisi significa scissione del glucosio. É una serie di reazioni, nove in tutto, mediante le quali il glucosio viene trasformato in due molecole di un composto a tre atomi di carbonio, la gliceraldeide 3-fosfato o fosfogliceraldeide (PGAl), e successivamente in due molecole di piruvato.
Questa serie di reazioni si svolge nel citoplasma, sia delle cellule procarioti che eucarioti, in assenza di ossigeno. Nella prima serie di tappe (dalla 1 alla 4), il glucosio viene trasformato in PGAl, previo utilizzo di due molecole di ATP. La tappa 3 è catalizzata dall'enzima fosfofruttochinasi; esso è un enzima fondamentale, soggetto a controllo allosterico. L'ATP, infatti, inibisce la sintesi di fruttosio 1,6-bifosfato, legandosi al sito regolatore dell'enzima, mentre l'ADP ne favorisce la sintesi, promuovendo così la prosecuzione della glicolisi. Questo meccanismo viene utilizzato dalle cellule per evitare di produrre ATP quando non serve.Il controllo della glicolisi avviene nella tappa 4, poiché il glucosio 6-fosfato, prodotto nella prima tappa, serva anche in altre vie metaboliche, come ad esempio la sintesi del glicogeno.
Bilancio finale della glicolisi
Per ogni molecola di glucosio che viene ossidata, la cellula ottiene 2 molecole di ATP (guadagno netto, dato che ne otterrebbe 4, ma 2 sono state utilizzate nelle tappe 1 e 3) e 2 molecole di NADH:glucosio + 2ATP + 4ADP + 2Pi + 2NAD+ → 2piruvato + 2ADP + 4ATP + 2NADH + 2H+semplificando i termini comuni, si ottiene:glucosio + 2ADP + 2Pi + 2NAD+ → 2piruvato + 2ATP + 2NADH + 2H+La glicolisi produce in tutto 598,3 Kjoule per mole di glucosio e produce il piruvato, che è una molecola che conserva ancora un notevole contenuto energetico (2272 Kjoule/mol).Il NAD+ deve essere rigenerato, altrimenti la glicolisi rallenta fino a fermarsi. L'ossidazione del NADH, che permette quindi il suo ripristino, può avvenire:
- in anaerobiosi, quindi per mezzo di processi fermentativi, nel citoplasma
- in aerobiosi, per mezzo della respirazione cellulare, nei mitocondri.
B) COENZIMI E Trasportatori
Cosa sono i Coenzimi?
Diversi enzimi per la loro azione catalitica necessitano dell'intervento di cofattori che partecipano attivamente alla reazione chiamati coenzimi.
Essi Sono molecole organiche dalla struttura spesso molto complessa, di natura non proteica, contengono nella loro struttura una vitamina o un suo derivato.
Per diventare coenzima, la vitamina subisce delle trasformazioni che vanno dalla semplice fosforilazione (uno dei casi più comuni) a trasformazioni più complesse
Possono essere divisi in due categorie :
1)Trasporto gruppi (H, Acile, Fosfato ecc) :Es. NAD NADP , FAD, FMN. , Acetil Coenzina A
2) Trasportatori di elettroni: Citocromi ecc.
Diversi enzimi per la loro azione catalitica necessitano dell'intervento di cofattori che partecipano attivamente alla reazione chiamati coenzimi.
Essi Sono molecole organiche dalla struttura spesso molto complessa, di natura non proteica, contengono nella loro struttura una vitamina o un suo derivato.
Per diventare coenzima, la vitamina subisce delle trasformazioni che vanno dalla semplice fosforilazione (uno dei casi più comuni) a trasformazioni più complesse
Possono essere divisi in due categorie :
1)Trasporto gruppi (H, Acile, Fosfato ecc) :Es. NAD NADP , FAD, FMN. , Acetil Coenzina A
2) Trasportatori di elettroni: Citocromi ecc.
ATP
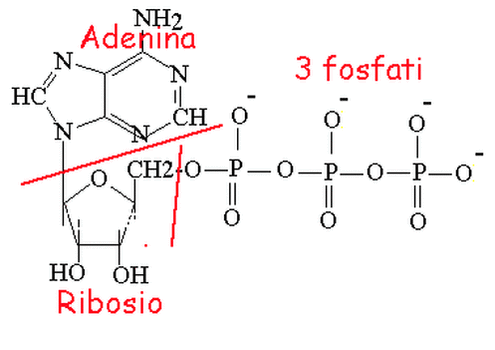
La 'moneta' per gli scambi energeticiL'istituzione di legami covalenti per formare ad esempio i polimeri che caratterizzano le cellule, avviene con consumo di energia. In qual modo avviene la fornitura dell'energia occorrente?
Protagonisti di questa fornitura sono i Ribonucleotidi trifosfati ed in particolare l'Acido adenosintrifosforico (sigla ATP ).
La molecola di questo singolare e importantissimo composto deriva dall'unione di una molecola di adenosindifosfato con una molecola di acido ortofosforico (H 3PO4, sigla P):
ADP + P + 29.3 KJoule → ATP Quando questa reazione decorre da sinistra verso destra (fosforilazione dell'adenosindifosfato) viene immagazzinata una quantità di energia che viene stimata intorno alle 29.3 kJoule per mole, la stessa quantità di energia viene ceduta quando la reazione decorre da destra verso sinistra (defosforilazione dell'adenosintrifosfato)
Per la facilità con cui immagazzina e cede una dose di energia, l'ATP viene anche indicato come 'moneta di scambio' del metabolismo dei viventi. Infatti, qualunque lavoro all'interno della cellula, sia che riguardi la sintesi di nuovi composti, sia che riguardi la motilità cellulare, o altri processi, avviene quasi sempre grazie alla defosforilazione dell'ATP. Solo in casi particolari la moneta di scambio può essere un altro ribonucleotide fosfato o un polifosfato, ma questa evenienza è piuttosto rara.Paragraph. Fai clic qui per effettuare modifiche.Paragraph. Fai clic qui per effettuare modifiche.
Protagonisti di questa fornitura sono i Ribonucleotidi trifosfati ed in particolare l'Acido adenosintrifosforico (sigla ATP ).
La molecola di questo singolare e importantissimo composto deriva dall'unione di una molecola di adenosindifosfato con una molecola di acido ortofosforico (H 3PO4, sigla P):
ADP + P + 29.3 KJoule → ATP Quando questa reazione decorre da sinistra verso destra (fosforilazione dell'adenosindifosfato) viene immagazzinata una quantità di energia che viene stimata intorno alle 29.3 kJoule per mole, la stessa quantità di energia viene ceduta quando la reazione decorre da destra verso sinistra (defosforilazione dell'adenosintrifosfato)
Per la facilità con cui immagazzina e cede una dose di energia, l'ATP viene anche indicato come 'moneta di scambio' del metabolismo dei viventi. Infatti, qualunque lavoro all'interno della cellula, sia che riguardi la sintesi di nuovi composti, sia che riguardi la motilità cellulare, o altri processi, avviene quasi sempre grazie alla defosforilazione dell'ATP. Solo in casi particolari la moneta di scambio può essere un altro ribonucleotide fosfato o un polifosfato, ma questa evenienza è piuttosto rara.Paragraph. Fai clic qui per effettuare modifiche.Paragraph. Fai clic qui per effettuare modifiche.
NAD e NADP
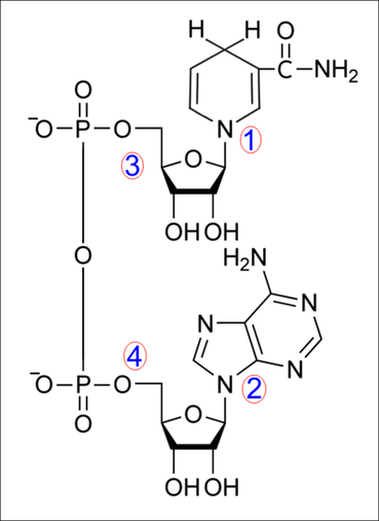
Nicotin-amide-dinucleotide -é costituito da:
La nicotinammìde (vitamina PP) è la parte indicata in figura dal numero 1. È proprio questa struttura che svolge il ruolo biologico generale della molecola, potendo essa donare/accettare atomi di idrogeno.
L'adenina è invece la struttura chimica indicata con il numero 2. Essa è presente negli acidi nucleici, essendo una delle cinque basi azotate, e si trova inoltre nell'ATP, nell'ADP e nell'AMP; essa è solitamente simboleggiata dalla lettera A, ed è una base detta purinica (6-amminopurina).
Il di-nucleotide consiste invece nella coppia di nucleotidi contrassegnata in figura dai numeri 3 e 4; in ciascuno di essi è presente un gruppo fosfato ed uno zucchero pentoso, il ribosio.
Il NADP differisce soltanto per la presenza di un terzo gruppo fosforico.
La NAD(P)H è un coenzima ossidoriduttivo facente parte della classe delle DEIDROGENASI l NADH/NAD, come coenzima ossidoriduttivo, agisce nelle reazioni redox ovvero in reazioni di ossidazione e riduzione, partecipandovi.
Le reazioni di ossidazione vedono impegnato il NAD+, in quanto riducendosi a NADH, accetta un protone (idrogenione H) e due elettroni (o più spesso un idruro H- , grazie al quale riceve direttamente un protone dell'idrogeno e due elettroni) dalla molecola substrato (generalmente indicata con la sigla SH2, dove S= substrato) e agevola quindi la sua ossidazione.
Mentre nella reazione di riduzione di un generico SH ad SH2, il coenzima si ossida da NADH a NAD+, donando un protone e due elettroni. La reazione di ossidazione è la favorita.
generica riduzione del substrato e ossidazione del coenzima
NADH + SH --> NAD+ + SH2
generica ossidazione di substrato (riduzione del coenzima):
NAD+ + SH2 ---> NADH + SH
La nicotinammìde (vitamina PP) è la parte indicata in figura dal numero 1. È proprio questa struttura che svolge il ruolo biologico generale della molecola, potendo essa donare/accettare atomi di idrogeno.
L'adenina è invece la struttura chimica indicata con il numero 2. Essa è presente negli acidi nucleici, essendo una delle cinque basi azotate, e si trova inoltre nell'ATP, nell'ADP e nell'AMP; essa è solitamente simboleggiata dalla lettera A, ed è una base detta purinica (6-amminopurina).
Il di-nucleotide consiste invece nella coppia di nucleotidi contrassegnata in figura dai numeri 3 e 4; in ciascuno di essi è presente un gruppo fosfato ed uno zucchero pentoso, il ribosio.
Il NADP differisce soltanto per la presenza di un terzo gruppo fosforico.
La NAD(P)H è un coenzima ossidoriduttivo facente parte della classe delle DEIDROGENASI l NADH/NAD, come coenzima ossidoriduttivo, agisce nelle reazioni redox ovvero in reazioni di ossidazione e riduzione, partecipandovi.
Le reazioni di ossidazione vedono impegnato il NAD+, in quanto riducendosi a NADH, accetta un protone (idrogenione H) e due elettroni (o più spesso un idruro H- , grazie al quale riceve direttamente un protone dell'idrogeno e due elettroni) dalla molecola substrato (generalmente indicata con la sigla SH2, dove S= substrato) e agevola quindi la sua ossidazione.
Mentre nella reazione di riduzione di un generico SH ad SH2, il coenzima si ossida da NADH a NAD+, donando un protone e due elettroni. La reazione di ossidazione è la favorita.
generica riduzione del substrato e ossidazione del coenzima
NADH + SH --> NAD+ + SH2
generica ossidazione di substrato (riduzione del coenzima):
NAD+ + SH2 ---> NADH + SH
FAD e FMN
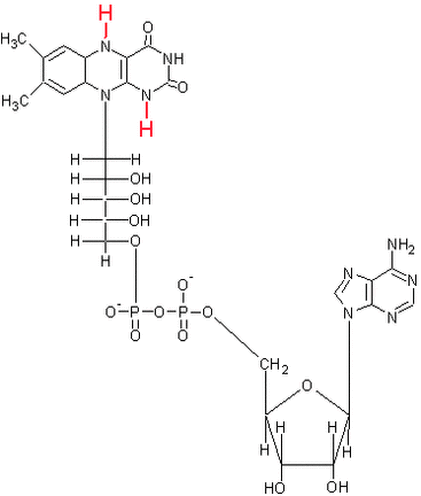
La flavina adenina dinucleotide (FAD o FADH2) deriva dalla vitamina B2 o riboflavina, è un importante fattore ossidante del ciclo di Krebs ed interviene nel trasporto degli elettroni nel processo biochimico chiamato catena di trasporto degli elettroni.
È un coenzima ossidoriduttivo e partecipa a innumerevoli reazioni che comportano il trasferimento di 1 o 2 elettroni.
La molecola è costituita da tre anelli condensati, che formano il cosiddetto il gruppo isoallosazinico della flavina, il quale è a sua volta legato al ribitolo (aldolo a cinque atomi di carbonio, ovvero il composto derivato dalla riduzione del ribosio) tramite l'atomo di azoto (N) dell'anello centrale.
La molecola di FMN contiene un solo gruppo fosforico e non contiene l'adenina e il ribosio.
Nella forma ridotta della molecola interviene in diverse reazioni biochimiche di trasporto degli elettroni e nella ossidazione degli acidi grassi.
Se all'anello ci sono legati due atomi di idrogeno, allora prenderà il nome di FADH2.
Durante il ciclo di Krebs, il FAD acquisisce due atomi di idrogeno, che si legano agli atomi di azoto con doppi legami negli anelli aromatici della riboflavina diventando FADH2, come mostra l'immagine del FADH2. Viene poi riossidata per passaggio degli elettroni ai citocromi, al coenzima q, o direttamente all'ossigeno nella catena respoiratoria.Paragraph.
È un coenzima ossidoriduttivo e partecipa a innumerevoli reazioni che comportano il trasferimento di 1 o 2 elettroni.
La molecola è costituita da tre anelli condensati, che formano il cosiddetto il gruppo isoallosazinico della flavina, il quale è a sua volta legato al ribitolo (aldolo a cinque atomi di carbonio, ovvero il composto derivato dalla riduzione del ribosio) tramite l'atomo di azoto (N) dell'anello centrale.
La molecola di FMN contiene un solo gruppo fosforico e non contiene l'adenina e il ribosio.
Nella forma ridotta della molecola interviene in diverse reazioni biochimiche di trasporto degli elettroni e nella ossidazione degli acidi grassi.
Se all'anello ci sono legati due atomi di idrogeno, allora prenderà il nome di FADH2.
Durante il ciclo di Krebs, il FAD acquisisce due atomi di idrogeno, che si legano agli atomi di azoto con doppi legami negli anelli aromatici della riboflavina diventando FADH2, come mostra l'immagine del FADH2. Viene poi riossidata per passaggio degli elettroni ai citocromi, al coenzima q, o direttamente all'ossigeno nella catena respoiratoria.Paragraph.
COENZIMA A
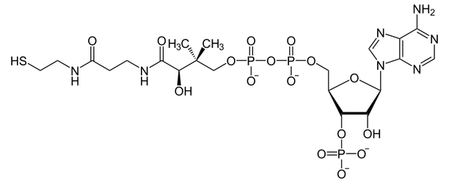
l Coenzima A é il più importente coenzima per il trasporto dei gruppi acile o acetile in forma "attivata".
Il gruppo trasportato è legato al gruppo funzionale tiolico (-SH) dellamercapto-etilammina mediante un legame tioestere.
Il legame tioestere è caratterizzato da un'elevata energia libera di idrolisi: è proprio grazie a questa caratteristica che le reazioni di trasferimento del gruppo acile o acetile possono procedere spontaneamente.
L'acido pantotenico é la componente vitaminica essenziale del coenzima (talvolta indicato come vitamina B5).
Nel coenzima A, l'acido pantotenico è legato mediante un legame estere al pirofosfato dell'ADP 3'-fosfato e mediante un legame ammidico al gruppo amminico della mercaptoetilammina.
L'acetil - Coenzima A é comune del metabolismo dei glucidi, dei lipidi e delle proteine per proseguire la respirazione cellulare con il ciclo di Krebs
CITOCROMI e CATENA TRASPORTO ELETTRONI
Le reazioni cataboliche determinano la sottrazione di elettroni dalle molecole di substrati ossidate.
Questi elettroni vengono transitoriamente convogliati sui coenzimi specifici (NAD+, NADP+ e FAD) delle varie deidrogenasi.
Gli elettroni legati ai coenzimi NAD+ e FAD sono in seguito trasferiti a specifici trasportatori di elettroni ed infine all’ossigeno, l’accettore finale.La catena di trasporto degli elettroni è costituita da una serie di trasportatori di elettroni, la gran parte dei quali sono proteine integrali di membrana, contenenti gruppi prostetici capaci di accettare o donare elettroni.
Quali sono le caratteristiche dei Citocromi?
Sono dei composti di natura proteica ,contenenti un gruppo eme, che trasportano gli elettroni nella catena di trasporto alla fine della respirazione cellulare.
Vi sono 3 classi di citocromi (a, b, c).
Nei citocromi a e b il gruppo eme è legato alla proteina non covalentemente.
Nei citocromi c il gruppo eme è legato covalentemente a residui di cisteina della proteina.
Nei citocromi b è presente lo stesso gruppo eme della mioglobina e della emoglobina.
Negli altri tipi di citocromi il gruppo eme presenta delle differenze.
I citocromi di tipo a e b, ed alcuni di tipo c, sono proteine integrali della membrana mitocondriale interna.
Un’eccezione è rappresentata dal citocromo c, una proteina solubile che si lega alla superficie esterna della membrana mitocondriale interna.
Nei citocromi l’atomo di ferro del gruppo eme può assumere stati di ossidazione Fe2+ o Fe3+.
Il gruppo trasportato è legato al gruppo funzionale tiolico (-SH) dellamercapto-etilammina mediante un legame tioestere.
Il legame tioestere è caratterizzato da un'elevata energia libera di idrolisi: è proprio grazie a questa caratteristica che le reazioni di trasferimento del gruppo acile o acetile possono procedere spontaneamente.
L'acido pantotenico é la componente vitaminica essenziale del coenzima (talvolta indicato come vitamina B5).
Nel coenzima A, l'acido pantotenico è legato mediante un legame estere al pirofosfato dell'ADP 3'-fosfato e mediante un legame ammidico al gruppo amminico della mercaptoetilammina.
L'acetil - Coenzima A é comune del metabolismo dei glucidi, dei lipidi e delle proteine per proseguire la respirazione cellulare con il ciclo di Krebs
CITOCROMI e CATENA TRASPORTO ELETTRONI
Le reazioni cataboliche determinano la sottrazione di elettroni dalle molecole di substrati ossidate.
Questi elettroni vengono transitoriamente convogliati sui coenzimi specifici (NAD+, NADP+ e FAD) delle varie deidrogenasi.
Gli elettroni legati ai coenzimi NAD+ e FAD sono in seguito trasferiti a specifici trasportatori di elettroni ed infine all’ossigeno, l’accettore finale.La catena di trasporto degli elettroni è costituita da una serie di trasportatori di elettroni, la gran parte dei quali sono proteine integrali di membrana, contenenti gruppi prostetici capaci di accettare o donare elettroni.
Quali sono le caratteristiche dei Citocromi?
Sono dei composti di natura proteica ,contenenti un gruppo eme, che trasportano gli elettroni nella catena di trasporto alla fine della respirazione cellulare.
Vi sono 3 classi di citocromi (a, b, c).
Nei citocromi a e b il gruppo eme è legato alla proteina non covalentemente.
Nei citocromi c il gruppo eme è legato covalentemente a residui di cisteina della proteina.
Nei citocromi b è presente lo stesso gruppo eme della mioglobina e della emoglobina.
Negli altri tipi di citocromi il gruppo eme presenta delle differenze.
I citocromi di tipo a e b, ed alcuni di tipo c, sono proteine integrali della membrana mitocondriale interna.
Un’eccezione è rappresentata dal citocromo c, una proteina solubile che si lega alla superficie esterna della membrana mitocondriale interna.
Nei citocromi l’atomo di ferro del gruppo eme può assumere stati di ossidazione Fe2+ o Fe3+.
