Stereochimica.
ISOMERI
Cos'é la stereochimica?
Con il termine stereochimica si intende lo studio delle proprietà spaziali delle molecole e come queste ultime si riflettano sul comportamento chimico delle sostanze.
Cosa sono gli Isomeri?
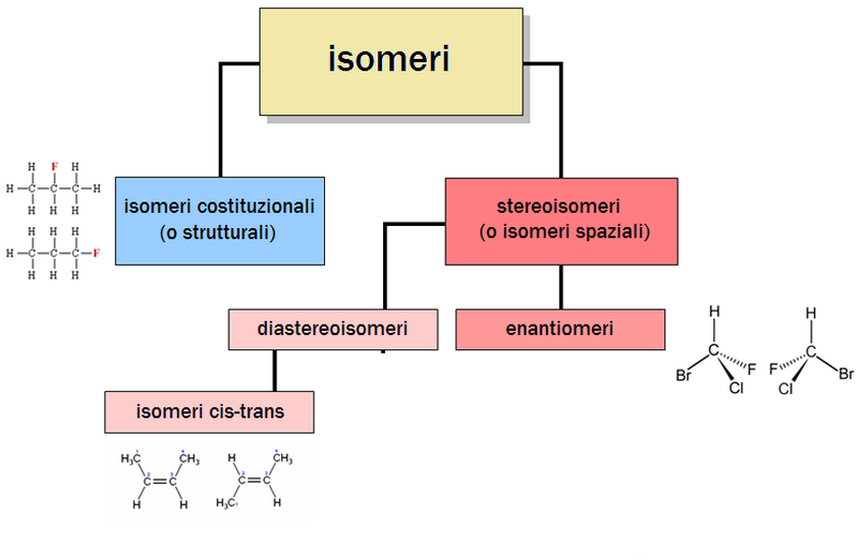
Due composti con medesima formula bruta si dicono isomeri. Questi possono essere:
- Isomeri costituzionali (o strutturali) :sono composti aventi la stessa formula molecolare ma diversa struttura. Il che implica differenti proprietà fisiche e chimiche, dovute ai legami differenti degli elementi che compongono la molecola.
- Stereoisomeri, se hanno formula bruta identica, ma la diversa orientazione spaziale degli atomi rende loro non sovrapponibili. Questi sono ulteriormente suddivisibili in:
- Enantiomeri, se hanno stessa connettività degli atomi, stessa formula chimica, oltre a possedere strutture speculari non sovrapponibili l'una all'altra.
- Diastereoisomeri, se possiedono stessa connettività degli atomi, stessa formula chimica, ma le molecole non sono strutture speculari.
ISOMERI STRUTTURALI
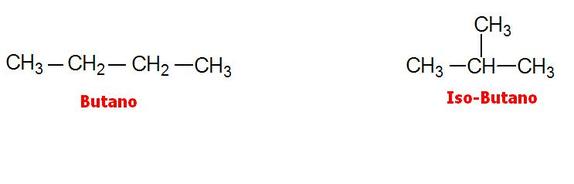
Isomeri Butano (C4H10)
Due isomeri di struttura sono formati dagli stessi atomi, che però possono essere legati tra loro in diverse combinazioni.
L’esempio più semplice di alcano ramificato che possiamo trovare in chimica organica è l’isobutano.
L’isobutano e il butano sono isomeri di struttura. Il butano in condizioni standard è un gas e ha punto di ebollizione -0,6 °C. Invece l’isobutano è il suo isomero che, pur avendo la stessa formula molecolare, ha caratteristiche chimico-fisiche diverse da quelle del butano normale: il suo punto di ebollizione, ad esempio, è -10 °C.
L’esempio più semplice di alcano ramificato che possiamo trovare in chimica organica è l’isobutano.
L’isobutano e il butano sono isomeri di struttura. Il butano in condizioni standard è un gas e ha punto di ebollizione -0,6 °C. Invece l’isobutano è il suo isomero che, pur avendo la stessa formula molecolare, ha caratteristiche chimico-fisiche diverse da quelle del butano normale: il suo punto di ebollizione, ad esempio, è -10 °C.
ISOMERIA OTTICA
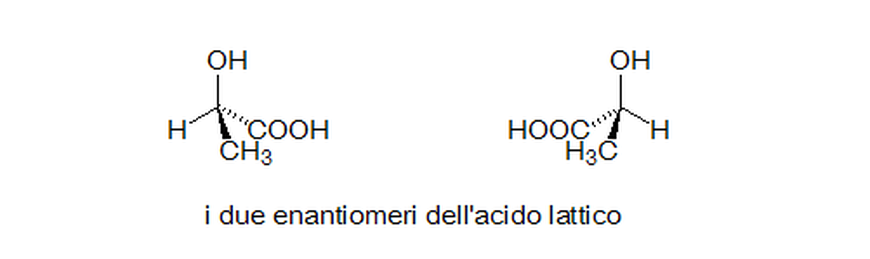
In cosa differiscono le due molecole di acido lattico?
Le due molecole riportate in questo esempio, differiscono solamente per il fatto di essere l'una l'immagine speculare , non sono sovrapponibili .
Due stereoisomeri che sono l'uno l'immagine speculare non sovrapponibile dell'altro si dicono enantiomeri in essi almeno un atomo di carbonio é legato a quattro gruppi diversi; un carbonio che ha questa caratteristica viene detto chirale.
Due isomeri ottici sono composti che presentano le stesse identiche proprietà fisiche e chimiche tranne una particolare proprietà ottica: se inseriamo una soluzione con i due isomeri ottici all'interno di un polarimetro, il fascio di luce polarizzata che verrà fatto passare sarà deviato verso destra e verso sinistra dello stesso angolo, rispetto alla retta che il fascio individuerebbe in assenza degli isomeri.
La luce polarizzata non verrà deviata se nel polarimetro inseriamo una soluzione contenente le stessa identica quantità dei due isomeri, ossia una soluzione "racemica"; solo in questo caso la luce continuerà a vibrare su un unico piano senza subire alcuna deviazione.
ISOMERIA GEOMETRICA O CIS_TRANS
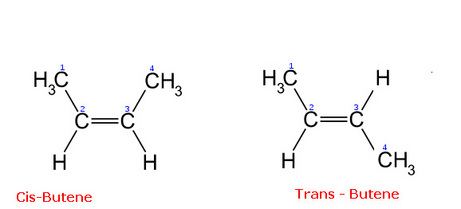
E' tipica dei composti che presentano dei doppi legami come ad esempio gli alcheni o come vedremo negli acidi grassi insaturi.
Affinché ci sia questa isomeria:
Gli isomeri geometrici vengono comunemente classificati con due diversi tipi di nomenclatura: cis e trans o Z e E.
Nella prima l'isomero cis è quello che ha due gruppi uguali dalla stessa parte di un doppio legame , il trans li ha da parti opposte.
I due isomeri cis e trans Butene hanno proprietà fisiche diverse:
Affinché ci sia questa isomeria:
- non deve esserci rotazione attorno al legame tra i due atomi di carbonio;
- ciascuno dei due atomi di carbonio deve essere legato a due gruppi diversi.
Gli isomeri geometrici vengono comunemente classificati con due diversi tipi di nomenclatura: cis e trans o Z e E.
Nella prima l'isomero cis è quello che ha due gruppi uguali dalla stessa parte di un doppio legame , il trans li ha da parti opposte.
I due isomeri cis e trans Butene hanno proprietà fisiche diverse:
- Cis- Butene punto ebollizione +4C° e punto fusione -130C°
- Trans- Butene punto ebollizione +1C° e punto fusione -104 C°
